勃林格殷格翰与北京大学肿瘤医院合作的BI 905711联合化疗Ⅰ期临床研究项目落地国内,成功入组全球首例患者
(医药健闻2022年1月26日讯)勃林格殷格翰与北京大学肿瘤医院合作的BI 905711联合化疗Ⅰ期临床研究项目落地国内,成功入组全球首例患者。

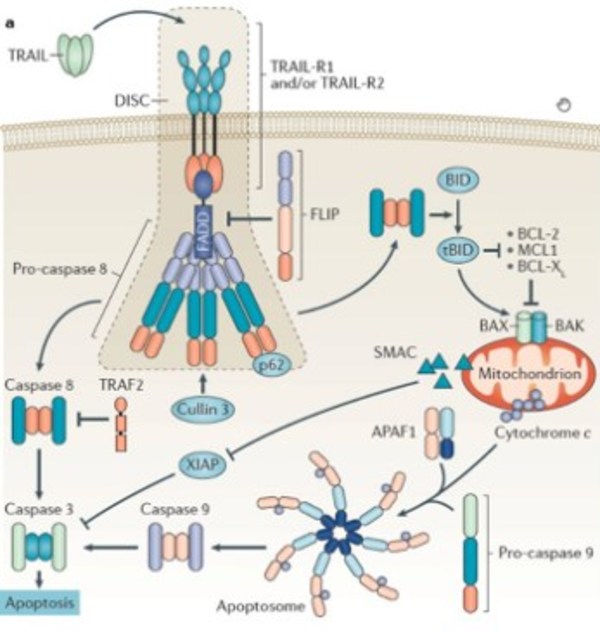
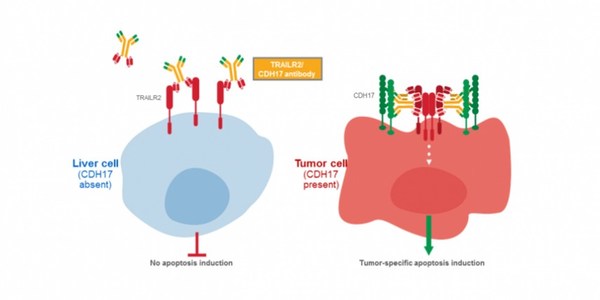
2022年1月,由中国消化肿瘤专家沈琳教授牵头开展晚期胃肠道癌症创新药物(促凋亡肿瘤坏死因子(TNF)相关凋亡诱导配体受体2(TRAILR2)/肿瘤细胞锚定钙粘蛋白17(CDH17)双特异性抗体BI 905711)相关临床研究,成功入组全球首例晚期胃肠道癌患者。BI 905711通过激活共同表达TRAILR2和CDH17的肿瘤细胞中的凋亡通路,从而遏制肿瘤进展。其结合了肿瘤靶向治疗和免疫治疗方法,为晚期消化道恶性肿瘤患者带来了新希望。
BI 905711作为一种首创的双特异性、四价抗体,其能够同时识别促凋亡肿瘤坏死因子(TNF)相关凋亡诱导配体受体2(TRAILR2)和肿瘤细胞锚定钙粘蛋白17(CDH17)。
TRAILR2是TNF受体超家族的成员,作为是一种促凋亡受体,在恶性肿瘤中广泛表达。其能有效地诱导多种肿瘤细胞系凋亡,但不会诱导大多数正常细胞凋亡。不仅如此,TRAILR2还可以通过与配体引发的低聚反应直接启动外源性凋亡途径,并具有与其它凋亡调控因子结合的潜能。
而CDH17作为钙黏蛋白超家族成员之一,具有特殊的结构特征。其主要表达于肠上皮细胞及部分胰腺导管上皮细胞,在细胞生长发育过程中起到重要作用。CDH17结构异常和功能紊乱会导致肿瘤细胞间粘附能力下降。组织细胞松散,易于脱落或变形,从而使瘤细胞获得更强的侵袭力,促进肿瘤的侵袭与转移。
BI 905711的作用机制正是依托上述在肿瘤细胞中高表达的特殊结构,识别在胃肠道中存在TRAILR2/CDH17共表达的肿瘤细胞,并激活其凋亡通路。从而达到控制肿瘤进展,促进肿瘤细胞凋亡的目的。
与此同时,研究发现其与化疗联合,能够通过激活肿瘤细胞的内源性和外源性凋亡途径来增强凋亡作用。在包括结直肠癌和胰腺癌在内的临床前胃肠道恶性肿瘤模型中,BI 905711单独给药以及与化疗药物联合用药时均显示出有效性。此外,研究还证实化疗药物预处理可使癌细胞对TRAILR2激动性抗体更为敏感,且序贯给药可克服耐药性。
基于上述“双管齐下”的抗肿瘤机制,BI 905711成为颇具前景的抗肿瘤候选药物。期待此次进行的Ⅰ期临床研究项目,能够获得良好的药物有效性及安全性数据。不仅为药物进一步开展后期临床试验提供依据,更能够为我国临床众多晚期消化道恶性肿瘤患者带来福音。