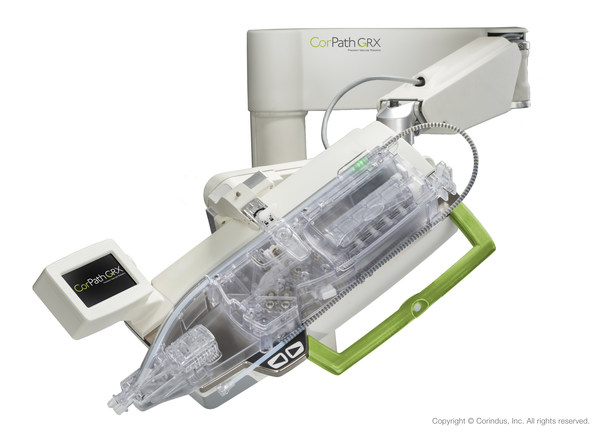
西门子医疗Corindus途灵(TM)介入手术机器人通过创新医疗器械特别审查申请
(医药健闻2021年8月2日讯)
西门子医疗Corindus途灵™最新一代CorPath® GRX介入手术机器人经国家药品监督管理局医疗器械技术审评中心创新医疗器械审查办公室组织的专家审查,通过创新医疗器械特别审查申请,于2021年7月30日获准进入特别审查程序。由此,西门子医疗成为首家通过创新医疗器械特别审查申请的外资医疗影像设备生产企业。
途灵适用于介入手术,可降低术中医患所受辐射剂量,提高手术操控精准度,可能减少医患的术中接触。与传统人工介入手术操作相比,途灵是具有根本性改进的领先医疗技术。在2020年第三届中国国际进口博览会上,途灵首次在中国正式亮相。2021年3月,在海南博鳌先行区政策的支持下,中国科学院院士、复旦大学附属中山医院葛均波教授及其团队在博鳌超级医院完成了中国首例途灵辅助下的冠状动脉介入治疗(PCI)手术,引发业内广泛关注。
为使这一领先医疗技术尽早造福中国患者与医生,西门子医疗积极筹备并提交了创新医疗器械特别审查程序的申请。日前,在创新医疗器械审查办公室组织的审查申请专家审评会上,西门子医疗中国区团队在会议现场远程连线位于美国的途灵总部团队成员,就途灵产品的安全性和有效性向评审专家进行了详细的阐述。同时,作为博鳌首例手术的操作者,葛均波院士团队的李晨光教授参与了评审会议,通过实际的术中操作体验,以及对技术细节的还原,为药监局评审专家答疑解惑。最终,途灵产品在技术上的根本性创新和临床价值的优势得到了药监局评审专家的一致肯定与认可。
《创新医疗器械特别审查程序》由药监局修订,旨在鼓励医疗器械的研发与创新、促进医疗器械新技术的推广和应用、推动医疗器械产业高质量发展,于2018年12月1日施行。在医疗器械进入特别审查程序后,药监局将在医疗器械满足审评基本要求的前提下,对创新医疗器械的审评和审批给予优先办理,同时药监局相关审评部门与专家将为创新医疗器械的注册与评审进行专项沟通与指导,优化注册与评审路径,从而加快创新医疗器械在中国的上市进程。
西门子医疗将积极配合药监局医疗器械技术审评中心,推动途灵尽快在中国上市,造福医患。“我们也将继续开拓创新,将更多先进的产品和技术在国内市场落地,为中国医疗事业的发展做出更大贡献。” 西门子医疗大中华区临床治疗系统副总裁浦峥嵘表示。